Beschreibung
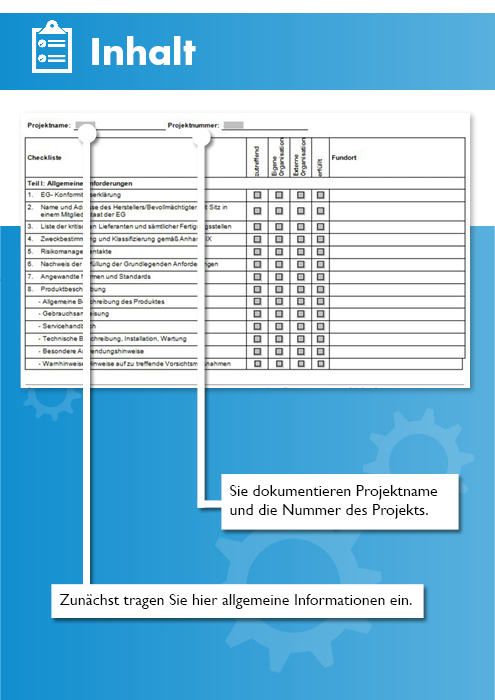
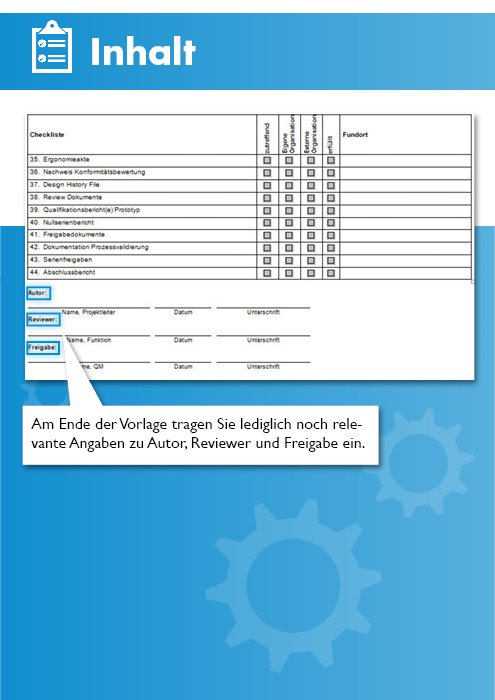
Nutzen Sie diese Checkliste Technische Dokumentation MDR, Anhang II und prüfen Sie, ob die Anforderungen der Medizinprodukteverordnung (MDR) 2017/745/EU an die technische Dokumentation bei Ihnen umgesetzt werden. In der Vorlage sind die einzelnen Anforderungen der Richtlinie aufgeführt. Sie können dann vermerken, ob diese Anforderungen für Ihre Organisation zutreffen und wer diese wie erfüllt. Die Checkliste für die technische Dokumentation gemäß der Medical Device Regulation (MDR) dient dazu, sicherzustellen, dass alle erforderlichen Informationen und Unterlagen für die Zulassung und den Betrieb eines Medizinprodukts gemäß den Anforderungen der MDR vorhanden sind. Sie unterstützt Hersteller dabei, die technische Dokumentation gemäß den regulatorischen Vorgaben vollständig und korrekt zusammenzustellen.
Außerdem erhalten Sie die umfangreiche Checkliste zu grundlegenden Sicherheits- & Leistungsanforderungen Anhang I, MDR. Das Ziel dieses Anhangs ist es, die Sicherheit und Leistung von Medizinprodukten in der Europäischen Union zu gewährleisten. Damit wird die Gesundheit und Sicherheit der Patienten, Anwender und Dritter geschützt.
Mit diesen Checklisten können Sie für Ihre Medizinprodukte die Erfüllung der Anhänge I (grundlegende Sicherheits- und Leistungsanforderungen) und II (technische Dokumentation) MDR überprüfen. Die grundlegenden Sicherheits- und Leistungsanforderungen umfassen verschiedene Aspekte, die für die Zulassung und den Vertrieb von Medizinprodukten in der EU erfüllt werden müssen. Diese sollen sicherstellen, dass die Produkte unter Berücksichtigung des Standes der Technik und der wissenschaftlichen Erkenntnisse entworfen und hergestellt werden. Mit dieser Checkliste überprüfen Sie einfach, ob Sie die Kriterien erfüllen.
Einfache Anpassung
Sie erhalten diese Checklisten selbstverständlich im offenen Dateiformat. Somit können Sie diese an das Design Ihres Unternehmens anpassen und direkt bearbeiten und vervielfältigen. Auch Verantwortlichkeiten können Sie direkt festlegen.
Wichtiger Hinweis: Sie erhalten diese Checklisten als englischsprachige Version. In der Praxis verfassen Unternehmen diese Dokumente zumeist in englischer Sprache, weshalb wir dies für diese Vorlage übernommen haben.
Sie sind auf der Suche nach einer ISO 13485 Schulung für Medizinproduktehersteller? Bei der VOREST AG stehen Ihnen über 130 Präsenzlehrgänge und über 100 E-Learning Kurse zur Verfügung.
Hier gleich unverbindlich und kostenlos den Gesamtkatalog oder den E-Learning Katalog downloaden.













Rezensionen
Es gibt noch keine Rezensionen.